Первый раз на Pharmnews.kz?
Войдите, чтобы читать, писать статьи и обсуждать всё, что происходит в мире. А также, чтобы настроить ленту исключительно под себя.
ЗарегистрироватьсяВойдите, чтобы читать, писать статьи и обсуждать всё, что происходит в мире. А также, чтобы настроить ленту исключительно под себя.
Зарегистрироваться
После того, как Администрацией США по продуктам питания и лекарствам (FDA) в препаратах метформина пролонгированного действия был обнаружен потенциальный канцероген N-нитрозодимметиламин (NDMA), вещество, которое может вызвать рак, уже седьмой по счету производитель лекарств объявляет об отзыве своего препарата из-за наличия NDMA.
23 сентября компания Sun Pharma объявила о добровольном отзыве одной партии препарата RIOMET ER™ (гидрохлорид метформина для пероральной суспензии с пролонгированным высвобождением, 500 мг на 5 мл). Причиной отзыва является уровень N-нитрозодимметиламина (NDMA), который оказался выше максимально допустимого суточного потребления, установленного FDA.
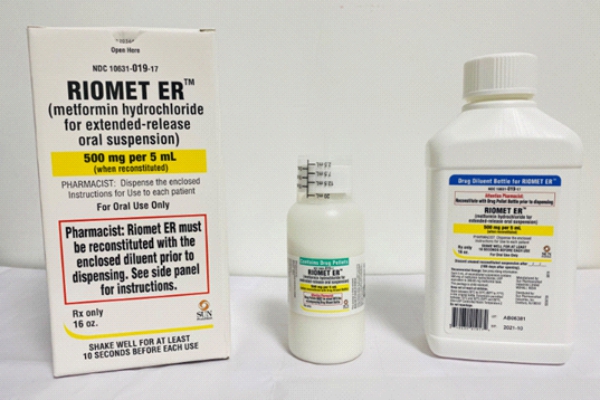
NDMA является известным загрязнителем окружающей среды и содержится в воде и продуктах питания, включая мясо, молочные продукты и овощи. До настоящего времени компания не получала никаких сообщений о неблагоприятных явлениях, связанных с этим препаратом.
RIOMET ER™ является рецептурным препаратом, применяется в качестве дополнения к диете и физическим упражнениям для улучшения гликемического контроля у взрослых и детей в возрасте 10 лет и старше с сахарным диабетом 2-го типа.
В отозванной партии содержится 747 флаконов со сроком годности до октября 2021 года.
Напомним, что на данный момент свои препараты метформина с рынка уже отозвали компании: Lupine, Granules, Apotex, Teva, Amneal и Marksans. Все препараты были пролонгированного действия.


 загружается...
загружается...
Комментарии
(0) Скрыть все комментарии