Первый раз на Pharmnews.kz?
Войдите, чтобы читать, писать статьи и обсуждать всё, что происходит в мире. А также, чтобы настроить ленту исключительно под себя.
ЗарегистрироватьсяВойдите, чтобы читать, писать статьи и обсуждать всё, что происходит в мире. А также, чтобы настроить ленту исключительно под себя.
Зарегистрироваться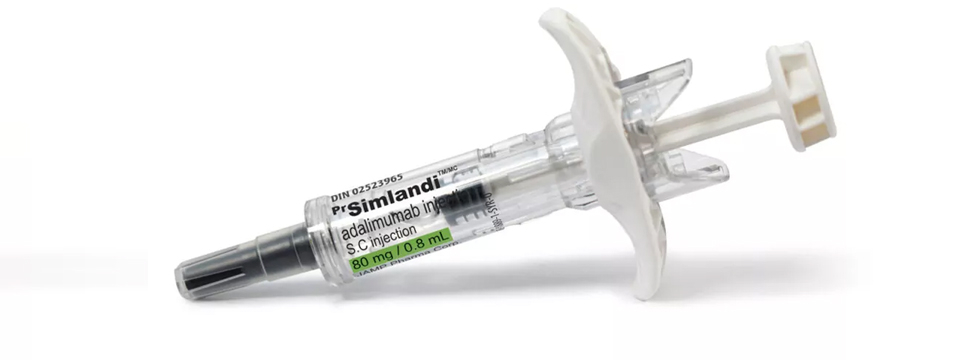
FDA одобрило препарат Simlandi от Teva и Alvotech – биоаналог Humira от AbbVie. Как и референтное лекарство, Simlandi разрешен для лечения ревматоидного артрита, ювенильного идиопатического артрита, псориатического артрита, анкилозирующего спондилита, болезни Крона, язвенного колита, бляшечного псориаза, гидраденита супуратива и увеита у взрослых.
Изначально Teva и Alvotech надеялись запустить в США свой биоаналог летом 2023 года, однако ввиду того, что инспекция FDA выявила проблемы на заводе Alvotech в Рейкьявике (Исландия), этим планам было не суждено сбыться. С тех пор на американском рынке появилось множество биоаналогов Humira, включая взаимозаменяемые копии от Pfizer и Boehringer Ingelheim, а также высококонцентрированные, но невзаимозаменяемые версии от Sandoz и других компаний.
Тем не менее, по словам генерального директора и председателя совета директоров Alvotech Роберта Вессмана, отличительной особенностью Simlandi является тот факт, что препарат повторяет высококонцентрированный формат Humira, на который приходится около 90% его продаж на американском рынке.
Учитывая его уникальный статус высококонцентрированного взаимозаменяемого биоаналога, ожидается, что Simlandi также получит рыночную эксклюзивность, добавил он. По мнению Вессмана, существующие биоаналоги Humira в США не получили большого распространения, поскольку они либо имеют низкую концентрацию, либо не являются взаимозаменяемыми.


 загружается...
загружается...
Комментарии
(0) Скрыть все комментарии